Реактор ИБР-2 поможет выяснить причины болезни Альцгеймера
По данным ВОЗ, в мире около 50 млн человек страдают деменцией. Наиболее распространенная форма — болезнь Альцгеймера: 60–70 % всех случаев. Известно о ней очень мало, лечения пока не существует. Чтобы узнать причины болезни Альцгеймера, в ОИЯИ экспериментируют с клеточными мембранами на реакторе ИБР‑2.
Фибриллы и одиночные пептиды
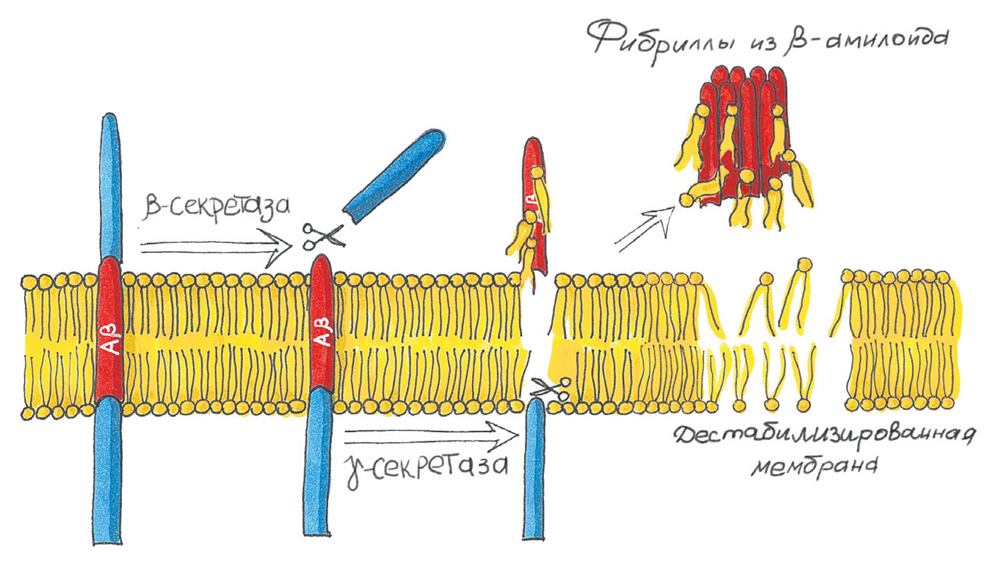
Болезнь Альцгеймера — первичная дегенеративная деменция. Из-за гибели нервных клеток головного мозга нарушаются когнитивные и физические способности. Почему и как возникает это заболевание, какие биологические и химические процессы лежат в его основе, ученые до сих пор не знают. Но есть несколько гипотез, одна из них, амилоидная, набрала популярность в последние годы. По ней, при расщеплении молекулы трансмембранного белка — предшественника бета-амилоида (ПБА) образуется пептид бета-амилоид. Его молекулы собираются в жесткие и нерастворимые фибриллы — амилоидные бляшки. В норме ПБА присутствует в мембранах нейронов и других клеток, его основная функция неизвестна. Однако исследования показали, что он задействован в образовании синапсов, антимикробной активности и транспорте железа через мембрану.
«О том, что у страдающих болезнью Альцгеймера в мозгу появляются фибриллы из пептида бета-амилоида, ученые узнали в XX веке. Но как и почему фибриллы формируются, какую роль играют — непонятно. Около 10 лет назад стали публиковать результаты, говорящие о том, что образование фибрилл — последствие процессов, которые происходят в мозгу пациентов с этой болезнью, а не ее причина. Но оказалось, помимо фибрилл есть и одиночные бета-амилоиды, которые, как мы думаем, взаимодействуют с мембранами клеток и разрушают их», — объясняет «СР» заместитель директора Лаборатории нейтронной физики ОИЯИ Норберт Кучерка.
В то время как фибриллы из бета-амилоида свободно циркулируют в межклеточных жидкостях, не нанося организму вреда, одиночные пептиды, полагают ученые, встраиваются в клеточную мембрану, каким-то образом с ней взаимодействуют, а затем выходят наружу, разрывая мембрану и уничтожая клетку. «Выход пептида из мембраны — это как раз то, чего нужно избежать, если мы хотим предотвратить болезнь, — отмечает Норберт Кучерка. — Нужно придумать, как его оставить в мембране либо как сделать так, чтобы он вообще не возникал. Моя научная группа и я сам довольно давно занимаемся изучением мембран, а в рамках этой работы начали исследовать, как взаимодействие бета-амилоида с мембраной зависит от ее свойств».
Эксперименты с мелатонином
Ученые создали везикулы — пузырьки, имитирующие клеточную мембрану. В среду, содержащую везикулы, добавляли холестерин, мелатонин и бета-амилоид и исследовали их влияние на структурные (толщина, площадь поверхности, уровень гидратации) и динамические (эластичность, диффузия) свойства мембраны, химические свойства липидов в ее составе.
Методы малоуглового рассеяния нейтронов и рентгеновских лучей и неупругое рассеяние нейтронов позволили исследовать характеристики биологических объектов, не разрушая их. Эксперименты проводили на установках ЮМО и НЕРА реактора ИБР‑2 в ОИЯИ и установке Rigaku в МФТИ.
«Мы смотрели, как ведет себя бета-амилоид сам по себе и в присутствии других веществ, которые содержатся в организме человека: холестерина и мелатонина. Холестерин входит в состав мембраны и делает ее более жесткой, а мелатонин, наоборот, делает мембрану более текучей. Исследовали также термодинамические свойства — при болезни Альцгеймера иногда резко поднимается температура, и из-за этого мембрана может менять характеристики. Узнали, что при добавлении пептидов везикулы меняют конформацию и становятся похожи на диски. Это просто удивительно. Единственное объяснение — мембрана действительно разрушается, потому что такой переход, морфологическое изменение, может произойти только из-за разрушения мембраны. И происходит это только при добавлении бета-амилоида», — рассказывает Норберт Кучерка.
Выяснилось также, что на встраивание пептидов в мембрану влияет ее вязкость — при добавлении мелатонина влияние пептида гораздо ниже, чем без него или при добавлении холестерина. Ученые предполагают, что мелатонин может защищать клетки и предотвращать болезнь Альцгеймера. Гипотеза требует исследований. В лаборатории продолжают работу, и, возможно, ее результаты помогут победить эту форму деменции.
КСТАТИ
Группа ученых из УрФУ, Института цитологии РАН и Института органического синтеза УрО РАН синтезировала химические соединения, способные остановить дегенерацию нейронов при болезнях Альцгеймера, Паркинсона и других тяжелых патологиях головного мозга. Новые молекулы рядов индолил и пирролилазинов активируют внутриклеточные механизмы борьбы с избытком амилоидных структур. Соединения запускают синтез особых белков теплового шока и вызывают их накопление в клетке. Белки этого типа позволяют обезопасить нейрональную ткань от амилоидов. Полученные соединения опробовали на клеточных моделях болезни Альцгеймера — новые вещества повысили выживаемость клеток. Наиболее эффективное соединение, пирролилазин, протестировали на крысах с вторичными повреждениями после черепно-мозговых травм. По словам ученых, это позволило животным избежать двигательных нарушений и дегенерации нейронов гиппокампа. Сейчас готовятся доклинические испытания.







