Подавить вредную транскрипцию: МИФИ ищет лекарство против опухолей мозга
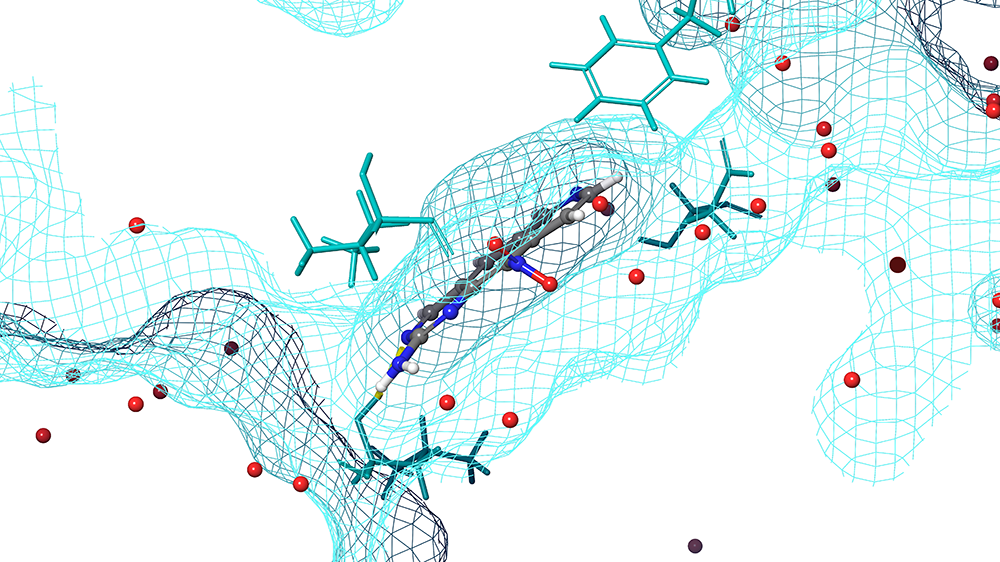
В Национальном исследовательском ядерном университете «МИФИ» изучают, как синтетические химические соединения подавляют функции жизненно важных для опухоли белков. Эта работа стала развитием давнего сотрудничества с французскими коллегами.
Ученые Института химии Университета Клермон-Оверни предложили искать ингибиторы развития злокачественной опухоли мозга (глиобластомы) среди особого класса искусственно синтезированных органических веществ — пиридохиназолинов. Эти гетероциклические низкомолекулярные соединения легко проникают сквозь биологические барьеры и взаимодействуют с белками-мишенями. А ученые МИФИ расчетными методами обосновали эффект подавления транскрипции генов в раковой клетке, достигаемый двумя близкородственными веществами этого класса.
«Мы отвечали за блок теоретических расчетов с использованием аппарата цифровой химии — инструментария современных вычислительных методов, при помощи которых решаются задачи на стыке точных и естественных наук, — говорит соавтор исследования София Борисевич, заместитель руководителя недавно открывшейся лаборатории хемоинформатики и молекулярного моделирования Института интеллектуальных кибернетических систем МИФИ. — Предмет нашего поиска — производные пиридохиназолинов, способные нанести серьезный урон раковой опухоли через воздействие на белки — серин-треониновые протеинкиназы. Эти ферменты регулируют множество жизненно важных клеточных функций, в том числе управляют транскрипцией генов в клетке злокачественной опухоли. Помешать транскрипции — значит нарушить процесс развития опухоли и в конечном счете помочь организму справиться с ней. Поэтому с пиридохиназолинами связывают большие надежды в разработке адресных противоопухолевых лекарств».
Согласно результатам молекулярного моделирования, два производных пиридохиназолинов оказались специфичны по отношению к двум белкам из семейства серин-треониновых протеинкиназ. Как по структуре, так и по химическому составу оба кандидата в лекарственные препараты очень близки. Эти молекулы различаются буквально парой атомов: в составе одной присутствует аминогруппа (NH2), в другой ее заменяет нитрогруппа (NО2). Оба агента борются с двумя протеинами, направляя удар на разные белковые мишени. Результаты расчетов хорошо согласуются с данными биологических экспериментов, проведенных в Институте биоорганической химии РАН им. Шемякина и Овчинникова.
«Международное сотрудничество в разработке противораковых препаратов продолжается, — комментирует руководитель лаборатории МИФИ Александр Штиль. — Предстоит найти ответы на многие важные вопросы. Подавить транскрипцию — неизбежно повредятся не только опухолевые, но и нормальные клетки. Выдержат ли они такое воздействие? Можно ли (и если да, то насколько) увеличить «терапевтическое окно» — где разница между лечебной и токсичной дозами лекарства? Поисками ответов на эти вопросы наш коллектив займется в ближайшем будущем».







